Pfizer a sciemment autorisé des composants dangereux dans ses vaccins

Le vaccin COVID-19 de Pfizer contient des fragments d'ARNm appelés «ARNm tronqués». Il s'agit d'un problème grave en plus des événements de sécurité potentiellement mortels du vaccin. Étonnamment, Pfizer a soumis des rapports d'analyse d'ARNm falsifiés à plusieurs autorités sanitaires.
La question de l'ARNm tronqué a conduit l'Agence européenne des médicaments (EMA) à soulever une "objection majeure" avant son approbation conditionnelle du vaccin en décembre 2020. Que s'est-il passé? Comment ces problèmes ont-ils été considérés comme résolus ? Cet article de la série en deux parties abordera la question en profondeur et examinera ses conséquences potentielles pour la santé humaine.
Résumé des principaux faits
- Le vaccin COVID-19 de Pfizer contient de l'ARNm tronqué, que l'EMA a signalé comme une raison de son "objection majeure", indiquant une exclusion de leur approbation.
- Pfizer n'a pas étudié les effets néfastes de l'ARNm tronqué dans ses vaccins.
- Pfizer a soumis des chiffres de transfert Western à la Food and Drug Administration (FDA) et à l'EMA qui ont été générés numériquement, et non à partir d'expériences réelles.
- Il y a eu un manque alarmant de mesures prises par les autorités sanitaires sur cette question.
- L'ARNm tronqué contribue potentiellement à de multiples blessures liées au vaccin, notamment des caillots sanguins fibreux induits par des protéines de pointe mal repliées, des troubles auto-immuns et le cancer.
- Ces problèmes avec le vaccin Pfizer auraient pu entraîner des variations drastiques de la qualité des produits d'un lot à l'autre. Cela pourrait expliquer la différence dans les événements indésirables subis par les vaccinés.
- La cause profonde d'une telle conduite irresponsable de la part des autorités pharmaceutiques et sanitaires est un manque d'éthique.
Lorsque vous allez au supermarché et que vous souhaitez acheter 10 bouteilles de lait entier pour vos enfants, vous supposez généralement que les produits chimiques et les concentrations dans ces 10 bouteilles sont identiques ou similaires. Personne ne s'attendrait à ce que cinq des bouteilles soient remplies de lait dilué tandis que les cinq autres étaient remplies de yaourt.
La plupart des aliments achetés en magasin répondent à nos attentes en raison de la réglementation et du contrôle de la qualité. Les mêmes critères existent également dans l'industrie pharmaceutique, y compris les produits vaccinaux.
Nous attendons des paramètres physiques et chimiques cohérents des ingrédients clés dans différents lots de médicaments ou de vaccins. La cohérence est le fondement qui permet aux patients et aux consommateurs d'avoir confiance dans l'innocuité et l'efficacité des médicaments.
Le processus CMC, abréviation de chimie, fabrication et contrôles, consiste à définir les pratiques de fabrication et les spécifications du produit qui doivent être suivies pour garantir la sécurité du produit et la cohérence entre les lots. Il s'agit d'un critère obligatoire pour les autorités sanitaires mondiales pour approuver un médicament ou un vaccin.
Contrôler la qualité d'un produit chimique traditionnel est relativement simple, mais pour un produit biologique, comme un ARNm, les choses se compliquent.
Qu'est-ce que l'ARNm tronqué? En quoi est-ce important?
Notre ADN contient des codes génétiques composés de nucléotides. L'ADN fabrique des protéines constituées d' acides aminés . Entre le code du gène et la protéine, il existe une molécule pont, un « traducteur », appelé ARN messager (ARNm).
La séquence d'ARNm pleine longueur du vaccin Pfizer codant pour la protéine de pointe a une longueur de 4 284 nucléotides .
Il consiste en une structure CAP en 5 'pour amorcer sa traduction en une protéine de pointe. Il fonctionne comme une boîte d'allumage d'une voiture. À la fin de la région traduisible, le cadre de lecture ouvert , il y a un codon d'arrêt, qui est comme les freins d'une voiture. Si un ARNm tronqué ne contient pas de codon stop, il ne parvient pas à donner un signal de « frein ». Le processus de traduction des protéines se poursuivra sans fin.
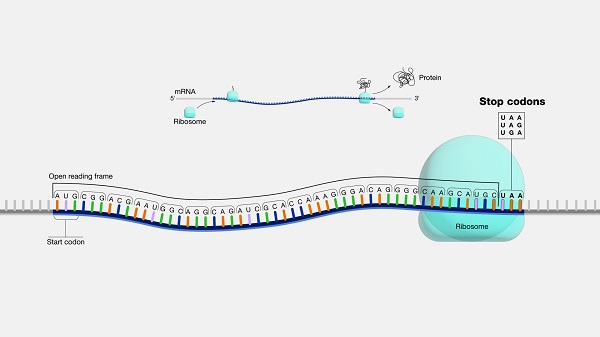
Une traduction d'ARNm en une protéine et le rôle du codon stop. (Avec l'aimable autorisation de l'Institut national de recherche sur le génome humain)
Le codon d'arrêt manquant de l'ARNm tronqué est très préjudiciable aux humains . Cela peut conduire à la production de produits protéiques toxiques .
Le vaccin COVID-19 de Pfizer contient de l'ARNm tronqué
L'EMA est chargée d'approuver tous les médicaments à usage humain en Europe, y compris les médicaments et les vaccins. Le comité des médicaments à usage humain (CHMP) est le comité de l'EMA chargé d'interpréter les avis de l'agence.
Dans un rapport d'évaluation de l'EMA portant le code EMA/CHMP/448917/2021 , l'EMA a demandé à Pfizer de traiter les impuretés de son produit vaccinal, que le rapport de l'EMA décrit comme « ARNm tronqué et modifié ».
Le rapport de Pfizer à l'EMA a clairement montré que le vaccin de Pfizer contenait des impuretés, comme indiqué par "Peak 1" dans le graphique ci-dessous, basé sur une capture d'écran de la page 14 du rapport d'août 2021 de l' EMA .
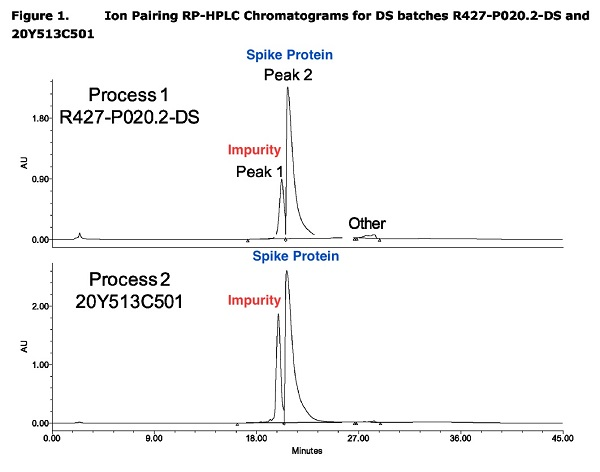
Le vaccin à ARNm de Pfizer contient des impuretés. (EMA)
L'EMA a exigé que Pfizer fournisse des données mensuelles sur le potentiel de génération de protéines/peptides de pointe tronqués ou d'autres protéines/peptides provoquant des maladies auto-immunes dues à des mécanismes de mimétisme moléculaire. Une date limite a été fixée à juillet 2021 et un rapport intermédiaire aurait dû être soumis d'ici mars 2021.
L'EMA a signalé l'ARNm tronqué comme une "objection majeure"
Dans un rapport d'évaluation de l'EMA sur "Comirnaty, COVID-19 mRNA vaccine (nucleoside-modified)", codé EMA/707383/2020, daté du 19 février 2021 , à la page 15 sous la section «Fabricant, contrôles de processus et caractérisation, » il est indiqué que « Au cours de la procédure, plusieurs problèmes ont été mis en évidence concernant le statut GMP de la fabrication de la substance active et les sites d'essai du produit fini aux fins de libération des lots. Ces problèmes ont été classés comme une objection majeure (MO).
Une « objection majeure » ??est un drapeau rouge réglementaire officiel émis par l'EMA. Si des objections majeures ne sont pas résolues, elles empêchent l'octroi de l'autorisation de mise sur le marché.

L'EMA a émis une objection majeure concernant le vaccin à ARNm de Pfizer. (EMA)
L'ARNm tronqué a été longuement discuté comme une "objection majeure" soulevée par l'EMA dans les deux rapports de l'EMA que nous avons analysés ci-dessus. Avant que ces agents biologiques ne soient déployés sur la population mondiale, les examinateurs de l'EMA ont identifié le problème de l'ARNm tronqué et l'ont soulevé comme une "objection majeure".
En juin 2022, Trial Site News a publié un rapport d'enquête révélant une diapositive divulguée présentée lors d'une réunion entre Pfizer-BioNTech et l'EMA. Alexandra (Sasha) Latypova, une ancienne dirigeante de l'industrie pharmaceutique qui a travaillé avec de nombreuses entreprises, dont Pfizer, a partagé la même diapositive dans sa sous-pile le 10 janvier 2023.
L'EMA a demandé à Pfizer de résoudre ces problèmes : « Les formes tronquées doivent être suffisamment caractérisées, c'est-à-dire qu'elles doivent être décrites, et il convient de discuter si les espèces fragmentées doivent être similaires entre les lots. En outre, la possibilité de protéines traduites autres que la protéine de pointe prévue (S1S2), résultant d'espèces d'ARNm tronquées et/ou modifiées, doit être abordée, et des données pertinentes sur la caractérisation des protéines doivent être fournies, si elles sont disponibles.

L'EMA a soulevé une objection majeure concernant la qualité de l'ARNm. (EMA)
Pfizer a reconnu l'ARNm tronqué dans ses vaccins
Pfizer a pleinement reconnu l'ARNm tronqué dans ses vaccins . La plupart des ARNm tronqués ont une longueur de 1 500 à 3 500 nucléotides avec un CAP en 5 ', sans la queue Poly (A) et le codon d'arrêt. Ils peuvent être traduits en une protéine de pointe partielle.
Malheureusement, lorsque l'ARNm arrive en fin de traduction, la chaîne d'acides aminés n'arrête pas la prolongation, car aucun signal d'arrêt ne leur a été donné. Il y a beaucoup d'ARNm dans la cellule. Comme il n'y a pas de signal d'arrêt, en théorie, un autre ARNm dans une cellule prendra le relais et poursuivra le travail inachevé, prolongeant la "protéine de pointe".
Si le même ARNm de pointe prend le relais, des protéines de type pointe prolongées avec plusieurs répétitions se formeront. Si un ARNm différent prend le relais, des types inconnus de protéines seront créés.
Le graphique annoté ci-dessous est basé sur une capture d'écran de la page 15 du rapport de l'EMA d'août 2021 .
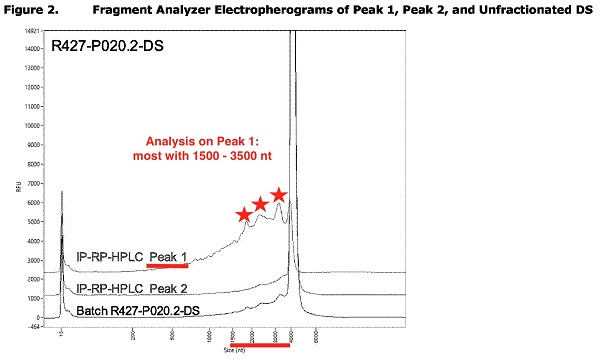
Le pic 1 contient les ARNm les plus tronqués de 1 500 à 3 500 nucléotides de long. (EMA)
Pfizer a également admis qu'il manquait une queue Poly(A) à l'ARNm tronqué. Le graphique annoté ci-dessous est basé sur une capture d'écran de la page 17 du rapport de l'EMA d'août 2021.
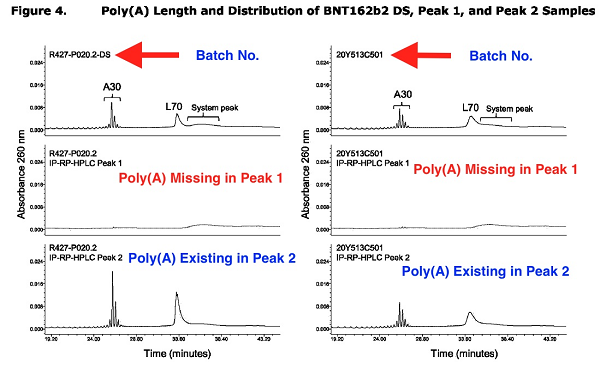
Il manque des queues Poly(A) au pic 1. (EMA)
De manière frappante, la proportion précise d'impuretés du pic 1 a été masquée dans ce rapport EMA téléchargé.
Le tableau annoté ci-dessous est basé sur une capture d'écran de la page 17 du même rapport de l'EMA.

Le pourcentage précis de Poly(A) dans le pic 1 a été masqué dans le rapport EMA téléchargé. (EMA)
Pfizer a soumis des chiffres numérisés Western Blot à la FDA et à l'EMA
Une méthode « Western blot » est utilisée pour identifier des protéines spécifiques, permettant aux chercheurs de vérifier la taille et l'abondance d'une protéine d'intérêt.
En raison des craintes qu'une protéine de pointe incorrecte puisse causer des blessures inattendues, l'EMA a demandé à Pfizer-BioNTech de soumettre des résultats expérimentaux pour démontrer que l'ARN du vaccin COVID-19 tronqué ne produirait pas de protéines fragmentées.
La demande de l'EMA est une préoccupation fondamentale et minimale à traiter pour tout produit d'ARNm destiné à un usage humain.
Cependant, comme il s'agit du premier cas d'utilisation de l'ARNm comme vaccin préventif pour une grande population, c'est aussi la première fois qu'un tel problème de qualité apparaît. Nous ne savons pas s'il existait auparavant une norme de qualité réglementaire pour gérer le risque d'ARNm tronqués.
La seule façon de caractériser ces fragments d'ARN est le séquençage. Pfizer n'a pas rapporté la séquence détaillée de ses ARNm tronqués dans son rapport, seulement le nombre approximatif de nucléotides.
En décembre 2020, Pfizer a fourni à la FDA des images de transferts Western qui exprimaient les niveaux de protéines de pointe induites par le vaccin COVID-19 et a affirmé que le vaccin ne produisait aucune autre protéine.
Un exemple de chiffre généré par Pfizer est présenté ci-dessous, basé sur une capture d'écran de la page 39 d' un rapport 2020 de la FDA . Pfizer a indiqué qu'il avait évalué la taille des protéines exprimées par le vaccin à ARNm et a conclu : "La taille des protéines exprimées est cohérente avec la taille attendue de la substance vaccinale à ARNm traduite et comparable dans tous les lots testés."
Cependant, le graphique apparaît numérique ou informatisé. Nous expliquerons la raison de notre évaluation plus loin dans cet article.

Transfert Western Pfizer 2020. (FDA)
Trois autres exemples de Western blots soumis en 2021 par Pfizer à l'EMA sont fournis ci-dessous.
Un Western blot a montré que l'ARNm tronqué dans le pic 1 ne génère pas de protéines in vitro. La figure annotée ci-dessous est basée sur une capture d'écran de la page 19 du rapport de l'EMA . Cependant, les Western blots sont des résultats numériques ou informatisés similaires à ceux présentés en décembre 2020 .
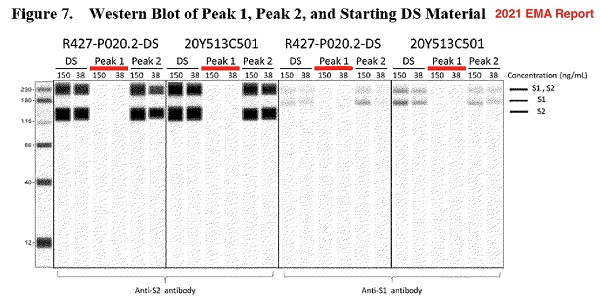
Graphique Western blot fictif soumis par Pfizer à l'EMA. (EMA)
Pfizer a utilisé les deux graphiques ci-dessous pour expliquer que les transcrits complets nécessitent Poly(A) pour l'expression ; cependant, les Western blots sont des résultats informatisés. La figure annotée ci-dessous est basée sur des captures d'écran de la page 18 du rapport EMA d'août 2021 .

Graphique Western blot fictif soumis par Pfizer à l'EMA. (EMA)
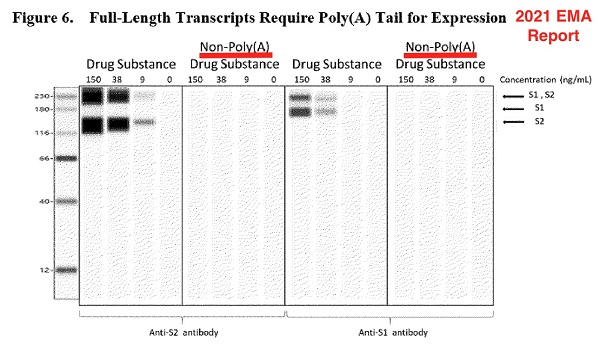
Graphique Western blot fictif soumis par Pfizer à l'EMA. (EMA)
Les transferts Western factices de Pfizer ont été soumis à des organismes de réglementation mondiaux, dont au moins la FDA , l'EMA et la Therapeutic Goods Administration (TGA) d'Australie .
Comment savons-nous que ces Western Blots ne sont pas réels ?
La première étape de la technique de transfert Western consiste à séparer les protéines d'un échantillon à l'aide d'un processus de biologie moléculaire appelé «électrophorèse sur gel».
Comme différentes protéines ont des tailles et des poids moléculaires différents, lorsqu'elles sont placées dans le même champ électrique, elles courent à des vitesses différentes d'un pôle à l'autre, comme une course à pied.
Au point de départ, les protéines sont réunies en une seule ligne, comme dans une course à pied de 400 mètres. Compte tenu d'un certain laps de temps, les plus petites protéines vont plus vite que les plus grosses, et progressivement, différentes protéines se sépareront à différents endroits, appelés «bandes». Ceci est similaire à ce qui se passe dans une course à pied : différents coureurs seront séparés les uns après les autres en fonction de leur vitesse dans une course à pied de 400 mètres.
Les facteurs qui déterminent l'apparition des Western blots comprennent la vitesse de transfert des protéines, le temps d'incubation et la concentration d'anticorps.
Par conséquent, dans la vraie vie, les Western blots sont rarement parfaits ; il y a toujours des distorsions.
Les Western blots « sourient » (courbent vers le haut sur les bords) un peu, saignent avec une queue et ont des bords arrondis et des barres inégales. Celles-ci sont souvent causées par le sel dans les échantillons ou par une forte concentration des protéines porteuses de charges électriques, modifiant ainsi l'intensité du champ électrique à leur voisinage et affectant leur migration.
Par exemple, le graphique Western blot (ci-dessous) du rapport EMA 2021 semble provenir d'une expérience réelle. Un artefact courant, tel qu'une bulle d'air entre le gel et la membrane de transfert, a probablement provoqué la tache lumineuse près du centre de la figure 8 au cours de l'expérience réelle. Les zones plus claires et plus sombres sont courantes.
Il s'agit du seul graphique Western blot du rapport de l'EMA qui semble provenir d'une "vraie" expérience. Cependant, Pfizer n'explique pas pourquoi il a soumis deux ensembles de graphiques Western blot à l'EMA dans le même rapport concernant le même problème.
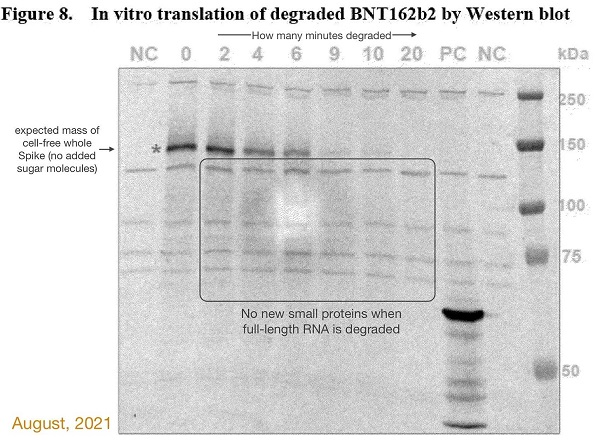
Exemple de Western blot des expériences Covid-19 BNT162b2 de Pfizer. (EMA)
De nombreux transferts Western fournis par Pfizer-BioNTech pour leurs protéines de pointe induites par le vaccin COVID-19 semblaient être impeccablement propres et parfaitement rectangulaires.
Les trois transferts Western (figures 5, 6 et 7) cités ci-dessus semblent faux - parfaitement réguliers, toutes les bandes restant bien dans leur voie; les taches sont entièrement sans bruit.
Epoch Times a contacté Pfizer pour un commentaire.
Le manque de données expérimentales ne permet pas une conclusion définitive ; Néanmoins, l'EMA l'a approuvé
Dans le même rapport, l'EMA a également écrit : « Il est probable que les espèces fragmentées n'aboutiront pas à des protéines exprimées, en raison de leur faible stabilité attendue et de leur faible efficacité de traduction (voir ci-dessous). Cependant, le manque de données expérimentales sur l'ARN tronqué et les protéines exprimées ne permet pas une conclusion définitive et nécessite une caractérisation plus poussée. Par conséquent, des données de caractérisation supplémentaires restent à fournir en tant qu'obligation spécifique (SO1).
Est-ce que quelqu'un interpréterait les faux rapports comme des données expérimentales fiables et leur ferait confiance pour soutenir l'approbation réglementaire ?

Le rapport EMA 2021 a déclaré qu'il manquait de données pour tirer une conclusion définitive. (EMA)
Néanmoins, aux pages 22 et 23 du rapport de l'EMA d'août 2021 , l'EMA a déclaré que ces problèmes étaient considérés comme résolus. Comment est-il considéré comme résolu ? Cette décision était-elle basée sur ces faux Western blots ?
L'EMA a accordé une autorisation de mise sur le marché conditionnelle à Pfizer/BioNTech le 12 décembre 2020 .
- Source : The Epoch Times (Etats-Unis)