Association entre la supplémentation en vitamine D et l'infection et la mortalité par COVID-19

Résumé
La carence en vitamine D a longtemps été associée à une fonction immunitaire réduite pouvant entraîner une infection virale. Plusieurs études ont montré que la carence en vitamine D est associée à une augmentation du risque d'infection par le COVID-19. Cependant, on ne sait pas si le traitement à la vitamine D peut réduire le risque associé d'infection au COVID-19, qui est au centre de cette étude. Dans la population d'anciens combattants américains, nous montrons que les remplissages de vitamine D 2 et D 3 étaient associés à des réductions de l'infection au COVID-19 de 28 % et 20 %, respectivement [(D 3 Hazard Ratio (HR) = 0,80, [IC 95 % 0,77, 0,83]), D2HR = 0,72, [IC à 95 % 0,65, 0,79]]. La mortalité dans les 30 jours suivant l'infection au COVID-19 était également inférieure de 33 % avec la vitamine D 3 et de 25 % avec la vitamine D2 (D 3 HR = 0,67, [IC à 95 % 0,59, 0,75] ; D 2 HR = 0,75, [IC à 95 % 0,55, 1,04]). Nous constatons également qu'après avoir contrôlé les taux sanguins de vitamine D, les anciens combattants recevant des doses plus élevées de vitamine D ont obtenu de plus grands avantages de la supplémentation que les anciens combattants recevant des doses plus faibles. Les vétérans dont les taux sanguins de vitamine D se situaient entre 0 et 19 ng/ml ont présenté la plus forte diminution de l'infection au COVID-19 après la supplémentation. Les vétérans noirs ont reçu une plus grande réduction du risque de COVID-19 associée à la supplémentation que les vétérans blancs. En tant que traitement sûr, largement disponible et abordable, la vitamine D peut aider à réduire la gravité de la pandémie de COVID-19.
Introduction
L'insuffisance et la carence en vitamine D affectent environ la moitié de la population américaine, avec des taux accrus chez les personnes à la peau plus foncée, une exposition réduite au soleil, les personnes vivant dans des latitudes plus élevées en hiver, les résidents des maisons de retraite et les travailleurs de la santé (1) . Les populations ayant de faibles niveaux de vitamine D ont également connu des taux plus élevés de COVID-19 (2,3,4,5,6).
Malgré plusieurs études indiquant une association entre de faibles niveaux de vitamine D et le COVID-19 (2,3,4,5,6,7), des informations limitées sont disponibles concernant le potentiel d'une supplémentation en vitamine D pour réduire le risque d'infection au COVID-19 . L'expansion de la supplémentation en vitamine D peut présenter une nouvelle et unique opportunité d'atténuer les taux d'infection mondiaux, étant donné qu'il s'agit d'un médicament en vente libre largement disponible, peu coûteux et associé à relativement peu d'effets secondaires.
Nous avons mené une étude pharmacoépidémiologique à grande échelle sur l'association entre la supplémentation en vitamine D 3 et D 2 et la probabilité d'infection au COVID-19 et d'infection au COVID-19 se terminant par une mortalité dans les 30 jours au Department of Veterans Administration (VA) dans le États-Unis. Nous avons également étudié si le sexe du patient, la race, les taux sériques de vitamine D et la dose cumulée de supplémentation en D 3 modifiaient l'association.
Arrière plan
Une infection COVID sévère est associée à des niveaux élevés de fragments de complément activés circulants (8) et à une réponse IFN gamma prolongée et améliorée produisant une réponse TH1 (9). Un complément excessif et l'IFN gamma sont des facteurs connus de lésions tissulaires (10,11). Les cellules épithéliales respiratoires infectées par le SRAS-CoV2 expriment et traitent le complément (C)3 pour générer C3a et C3b (12). C3b lie le récepteur CD46 sur les lymphocytes T CD4 + pour conduire la différenciation TH1 normalement suivie de leur arrêt. La séquence habituelle implique la production d'IFN gamma seul, puis d'IFN gamma plus IL10, et enfin d'IL10 seul (13). La production d'IL10 par les cellules TH1 est essentielle à la régulation de l'inflammation (14). Chauss et al. ont récemment identifié une boucle de vitamine D autocrine/paracrine qui permet aux cellules TH1 d'activer et de répondre à la vitamine D dans le cadre du programme cellulaire pour arrêter l'IFN gamma et améliorer l'IL10 (15). Cette découverte suggère que l'ajout de vitamine D à d'autres agents immunomodulateurs peut être utile chez les patients infectés par le SRAS-CoV2.
Plusieurs études observationnelles ont montré une forte relation entre l'infection par le COVID-19 et les faibles taux sériques de vitamine D (2,3,4,5,6,7). Une première étude de 489 patients avec des valeurs de laboratoire de vitamine D dans l'année précédant un test COVID-19 a révélé un risque accru de 77% d'un test COVID-19 positif chez les personnes présentant une carence en vitamine D (25-hydroxycholécalciférol inférieur à 20 ng / ml ou 1,25-dihydroxycholécalciférol moins de 18 pg/mL) (2). Une étude distincte a révélé un risque accru de 59 % de symptômes graves d'infection au COVID-19 chez les personnes ayant de faibles niveaux de vitamine D (25-hydroxycholécalciférol inférieur à 30 ng/mL) (3). En utilisant le même seuil, une troisième étude a révélé une augmentation de 45 % de l'infection au COVID-19 et une augmentation de 95 % des hospitalisations qui en résultent (4). Un quatrième rapport a révélé une augmentation de 35 % des taux d'infection au COVID-19 chez les patients présentant une carence en vitamine D (< 20 ng/mL) par rapport à ceux entre 30 et 34 ng/mL et une augmentation de 53 % par rapport à ceux ayant des valeurs ≥ 55 ng/mL. mL (5). Une cinquième étude d'observation à grande échelle en Israël a encore confirmé les découvertes précédentes (6). Plus généralement, la vitamine D est connue depuis longtemps pour améliorer la réponse immunitaire des patients. Une méta-analyse de 25 essais cliniques contrôlés randomisés (ECR) a identifié une diminution de 12 % des infections aiguës des voies respiratoires chez les patients recevant une supplémentation en vitamine D (16).
Deux essais contrôlés randomisés ont testé la capacité de la vitamine D à améliorer les résultats chez les patients déjà infectés par le COVID-19. Tout d'abord, une petite étude en ouvert a randomisé 76 patients infectés par le COVID-19 selon un rapport de 2: 1 pour un traitement par calcifediol oral (un analogue de la vitamine D 3 ) ou uniquement un traitement standard. Sur les 50 patients du groupe d'intervention, un seul (2 %) a dû être admis aux soins intensifs. En revanche, 26 (50 %) des patients du groupe de traitement standard ont dû être admis aux soins intensifs (17). Un deuxième essai contrôlé randomisé de traitement avec une seule dose orale élevée (200 000 UI) de calcifediol oral chez 240 patients hospitalisés n'a trouvé aucune réduction de la durée du séjour (18). Une nouvelle analyse ultérieure a révélé une réduction de 52 % des admissions en soins intensifs et une réduction de 60 % de l'utilisation de la ventilation mécanique uniquement chez les patients du groupe d'intervention avec des valeurs de 25(OH)D ≥ 20 ng/mL (19).
Une méta-analyse récente a montré une association entre de faibles taux sériques de 25-hydroxyvitamine D et la sensibilité, la gravité et la mortalité liées au COVID-19 (20).
Plus récemment, une étude de cohorte rétrospective de tous les patients hospitalisés pour COVID-19 en Andalousie (n = 15 968) a révélé une réduction de 33 % de la mortalité lorsque le calcifediol (c'est-à-dire de la vitamine D 2 ) était prescrit 15 jours avant l'hospitalisation et une réduction de 25 % de la mortalité. pour le cholécalciférol (c'est-à-dire la vitamine D 3 ) (21). Les réductions étaient de 27 % et de 12 % lorsque la fenêtre a été étendue à 30 jours avant l'hospitalisation. Une deuxième étude récente en Israël (n = 253 patients avec des niveaux de vitamine D avant l'infection) a trouvé une augmentation de 14 fois de la maladie COVID-19 sévère ou critique chez les patients présentant une carence en vitamine D (< 20 ng/ml) par rapport aux patients avec taux normaux de vitamine D (> = 40 ng/ml), ajustés selon l'âge, le sexe, l'IMC et les comorbidités (22).
Malgré les découvertes susmentionnées d'une association entre la carence en vitamine d et l'infection au COVID-19, il existe d'autres études qui remettent en question l'importance de cette découverte en plus de la relation entre la supplémentation en vitamine D et le COVID-19. Une méta-analyse de trois études récentes n'a trouvé aucune relation entre la supplémentation en vitamine D et la mortalité par COVID-19 en cas d'infection (23). Une autre méta-analyse a expliqué qu'une grande partie des preuves issues d'études observationnelles qui ont trouvé une association inverse entre les niveaux de vitamine D et le risque, la gravité et la mortalité d'infection au COVID-19 étaient faibles, et que davantage d'essais contrôlés randomisés étaient nécessaires pour clarifier la relation (24). Une troisième méta-analyse n'a pas été en mesure d'identifier une relation statistiquement significative entre la supplémentation en vitamine D et le risque d'infection au COVID-19, la mortalité et les admissions aux soins intensifs (25).
Compte tenu des résultats mitigés de la littérature, il est nécessaire de poursuivre les recherches sur la supplémentation en vitamine D en tant que prophylaxie ou traitement de l'infection au COVID-19, y compris les réductions potentielles de la mortalité. Nous étendons l'analyse de cette association en analysant une grande cohorte d'anciens combattants militaires américains, en comparant ceux prescrits de la vitamine D 3 et D 2 en termes de risque d'infection au COVID-19 et de mortalité à des témoins appariés.
Méthodes
Étudier le design
Nous avons mené une étude de cohorte rétrospective pour déterminer l'association entre la supplémentation en vitamine D 3 et D 2 et l'infection au COVID-19 et la mortalité. Nous avons estimé l'association en utilisant une cohorte de patients AV qui ont reçu une supplémentation en ergocalciférol (c'est-à-dire vitamine D 2 ), doxercalciférol (c'est-à-dire vitamine D 2 ), cholécalciférol oral (c'est-à-dire vitamine D 3 ) ou calcifediol (c'est-à-dire vitamine D 3) pendant une période avant la pandémie (c'est-à-dire du 1er janvier 2019 au 31 décembre 2020) et pendant la pandémie (c'est-à-dire du 1er mars 2020 au 31 décembre 2020) et des patients témoins non traités. Avant l'estimation, nous avons apparié les patients traités et témoins individuellement sur leur propension à la supplémentation séparément pour la vitamine D 3 et D 2 . Nous avons ensuite utilisé les modèles de risques proportionnels de Cox pour calculer le délai avant l'infection au COVID-19 et la mortalité dans les 30 jours suivant l'infection, sous réserve de supplémentation . Nous avons également effectué des analyses de sous-groupes pour D 3pour déterminer l'hétérogénéité du traitement selon la race (Noir contre Blanc), le taux de vitamine D (0–19 ng/ml, 20–39 ng/ml et 40 + ng/ml de 25-dihydroxycholécalciférol) et la dose moyenne quotidienne et cumulée de supplémentation. La plus petite taille de l'ensemble de données D 2 a empêché les analyses de sous-groupes.
Population étudiée
Nous avons identifié les patients VA avec au moins un service ou une ordonnance VA et au moins un test de laboratoire de vitamine D entre le 1er janvier 2019 et le 31 décembre 2020, dans les dossiers de santé électroniques de l'entrepôt de données d'entreprise (CDW) de l'administration des anciens combattants. Parmi la population traitée, les patients recevant à la fois des prescriptions de vitamine D 3 et D 2pendant la période active ont été abandonnées pour réduire les retombées entre les associations. De plus, les patients dont la première prescription a eu lieu pendant la pandémie ont été retirés de l'échantillon car il est peu probable que ces patients aient été exposés au traitement suffisamment longtemps pour obtenir une protection significative. (Les niveaux de vitamine D répondent généralement au traitement après deux mois d'exposition). Cette restriction a également réduit le potentiel de sélection des patients pour le traitement ; les patients prenant des mesures préventives, telles que l'initiation d'une supplémentation pendant la pandémie, pourraient être plus susceptibles d'adopter d'autres comportements préventifs (par exemple, le port de masque) qui confondraient l'association entre le traitement et l'infection au COVID-19 et la mortalité. Cela a également éliminé la possibilité d'un biais d'immortalité; infection pendant la pandémie, mais avant la supplémentation en vitamine D, ne pouvait pas être compté. Après application de toutes les restrictions, nous avons identifié 220 265 patients supplémentés en vitamine D3, 34 710 supplémentés en vitamine D 2 et 407 860 patients non traités.
Nous avons utilisé l'appariement des scores de propension un à un à partir de notre échantillon restreint de patients pour apparier les patients traités à la vitamine D 3 et à la vitamine D 2 aux témoins séparément. Les covariables utilisées pour générer les scores de propension comprenaient les 15 indications les plus courantes pour les remplissages de prescription de vitamine D (voir le tableau 1 ) et les données démographiques des patients (c'est-à-dire l'âge, la race et le sexe). La race des patients (c'est-à-dire, asiatique, noir, amérindien, autre race, blanc) et le sexe (c'est-à-dire, homme et femme) comprenaient tous les groupes disponibles signalés directement à partir des dossiers de santé électroniques CDW du ministère des Anciens Combattants. Après appariement, nous avons obtenu 199 498 paires témoins traitées à la vitamine D 3 et appariées et 33 216 paires témoins traitées à la vitamine D 2 et appariées.
Tableau 1 Échantillon de patients avant et après appariement.
Tableau pleine grandeur
En plus de notre analyse principale qui incluait tous les patients traités et témoins, nous avons également créé des cohortes de patients stratifiées par sexe (homme ou femme), race (noir ou blanc) et taux sériques de vitamine D (c'est-à-dire 0 à 19 ng/ml, 20–39 ng/ml et 40 + ng/ml). Les patients noirs ont généralement une carence en vitamine D et des taux d'infection au COVID-19 plus élevés et peuvent bénéficier d'une supplémentation plus que les patients d'autres races (26). Il a également été constaté que les hommes avaient des taux sanguins de vitamine D inférieurs à ceux des femmes (27). De même, les patients dont les taux sériques de vitamine D sont plus faibles peuvent bénéficier davantage d'une supplémentation que les patients dont les taux sont plus élevés. De plus, les patients recevant des doses plus élevées sont plus susceptibles d'augmenter leurs taux sériques aux niveaux nécessaires à la protection contre le COVID-19 que les patients recevant des doses plus faibles (28). Dans notre échantillon de vitamine D 3 , nous avons identifié 359 081 hommes et 39 915 femmes, 71 071 patients noirs et 283 248 patients blancs, et 69 067 patients dont la première valeur de laboratoire sérique en vitamine D était comprise entre 0 et 19 ng/ml au cours de l'étude, 228 093 entre 20 et 39 ng/ml et 101 836 avec 40 + ng/ml. Nous n'avons pas créé de sous-groupes pour la vitamine D 2 car la taille de la population était trop petite pour produire des estimations fiables.
Exposition
La principale exposition était la supplémentation en vitamine D 3 ou D 2 survenant avant et après le début de la pandémie le 1er mars 2020. Les patients qui n'ont jamais reçu de vitamine D 3 ou D 2 ont servi de groupe de référence (c'est-à-dire de groupe témoin). Nous avons inclus tous les produits et dosages de vitamine D 3 ou D 2 dans les dossiers de santé électroniques du CDW, y compris les produits combinés contenant de la vitamine D 3 , comme les multivitamines.
Pour étudier la variation de l'association entre le traitement et l'infection au COVID-19 par les taux sériques de vitamine D, nous avons construit une variable catégorique représentant différents seuils de 25-dihydroxycholécalciférol (c'est-à-dire 0-19 ng/ml, 20-39 ng/ml et 40 + ng/ml). Le taux sanguin utilisé pour créer la variable catégorielle était la valeur du premier test de laboratoire de 25-hydroxyvitamine D au cours de la période d'étude (c'est-à-dire du 1er janvier 2019 au 31 décembre 2020) pour chaque patient (c'est-à-dire traité et témoin).
Nous avons créé deux mesures de dosage pour étudier le potentiel d'une relation dose-réponse. La première mesure, la dose cumulative, a été construite en multipliant chaque dose de prescription par les jours fournis. Nous avons ensuite agrégé les valeurs résultantes de toutes les ordonnances remplies par les patients pendant la pandémie (c'est-à-dire du 1er mars 2020 au 31 décembre 2020). La deuxième mesure était la dose quotidienne moyenne, pondérée par les jours fournis pendant la pandémie. Les options posologiques comprenaient 20 UI, 40 UI, 100 UI, 125 UI, 200 UI, 250 UI, 400 UI, 500 UI, 800 UI, 1 000 UI, 2 000 UI, 5 000 UI, 8 000 UI et 50 000 UI. Compte tenu des valeurs de dosage importantes et des distributions asymétriques pour les deux mesures, nous avons utilisé le logarithme naturel pour notre analyse (voir le tableau S3 ).
Résultats
Le résultat principal était une infection au COVID-19 confirmée en laboratoire, telle que mesurée par tout dossier médical VA ou demande d'assurance-maladie contenant un diagnostic pour le code U07.1 de la CIM-10. Nous avons également examiné le COVID-19 se terminant par la mortalité en tant que résultat secondaire. Nous avons défini COVID-19 se terminant par la mortalité comme tout décès dans les 30 jours suivant l'infection. Bien que les données des certificats de décès n'étaient pas disponibles et seraient préférables, la mortalité survenant peu de temps après l'infection est susceptible d'être fortement corrélée à la mortalité réelle due au COVID-19.
Analyses statistiques
Nous avons utilisé un modèle à risques proportionnels de Cox pour comparer séparément les vitamines D 3 et D 2groupes de supplémentation à des témoins appariés concernant le délai de diagnostic de COVID-19 et le délai de diagnostic de COVID-19 suivi de la mortalité dans les 30 jours. Les estimations des modèles à risques proportionnels de Cox sont exprimées en termes de rapports de risque, qui sont des mesures du risque instantané d'un résultat particulier à un moment donné. Pour le modèle de diagnostic du délai jusqu'au COVID-19, nous avons censuré tous les patients à la date d'un diagnostic COVID-19 confirmé en laboratoire, de la mortalité ou de la fin de la période d'étude le 31 décembre 2020. Diagnostic COVID-19 suivi du modèle de mortalité dans les 30 jours, nous avons censuré les patients sur la mortalité ou la fin de la période d'étude. Nous avons ensuite répété l'analyse du diagnostic du délai avant COVID-19 dans notre vitamine D 3cohorte traitée et témoin en utilisant des stratifications par race (noir contre blanc), sexe (homme contre femme), taux sériques de vitamine D (0–19 ng/ml, 20–39 ng/ml et 40 + ng/ml). En termes de race, nous avons réalisé une analyse complémentaire pour estimer l'interaction race par traitement, avec et sans ajustement du taux sérique de vitamine D. Nos analyses dose-réponse qui utilisaient la vitamine D 3 cumulative et la dose quotidienne moyenne ont été estimées dans l'ensemble de l'échantillon et dans les stratifications sériques. Enfin, nous avons effectué une analyse de sensibilité qui contrôlait la saisonnalité en tant que covariable variant dans le temps.
Nous avons effectué toutes les analyses à l'aide de STATA-17.
Cette étude (VA MIRB # 00701, PI Jill Lavigne) a été examinée et approuvée en vertu de la détermination d'exemption de catégorie 4 par le Syracuse VA Medical Center Institutional Review Board à Syracuse, New York, et le VIREC Office for Medicare data de la VA. Cette recherche ne répondait pas aux critères de recherche sur des sujets humains, car les données de l'entrepôt d'entreprise VA et les demandes d'assurance-maladie sont anonymisées , de sorte qu'un consentement éclairé n'était pas requis. Toutes les méthodes ont été réalisées conformément aux directives et réglementations en vigueur.
Résultats
Avant l'appariement, il y avait des différences significatives dans la proportion de patients VA noirs et blancs, de patients carencés en vitamine D et de patients souffrant de dépression. Suite à l'appariement, les groupes supplémentés en vitamine D3 et témoins étaient similaires pour tous les facteurs de confusion potentiels (voir tableau 1 ) . Une plus grande proportion de patients noirs ont reçu de la vitamine D 2 par rapport à D 3 . En général, les patients recevant de la vitamine D 3 présentaient davantage de comorbidités que ceux recevant de la D 2 , voir Tableau 1 .
Pour s'assurer que les patients étaient bien appariés sur les caractéristiques observables susceptibles de prédire la supplémentation, nous avons évalué l'équilibre covariable et le soutien commun entre la supplémentation et les patients témoins après appariement. Le soutien commun a été évalué en divisant le score de propension en centiles et en comparant les patients traités et témoins avant l'appariement. L'équilibre des covariables a été déterminé en divisant l'échantillon en quintiles sur la base du score de propension et en comparant les sous-échantillons traités et témoins par chaque covariable dans chaque quintile. Un support commun du score de propension entre les sujets traités et les sujets témoins et un équilibrage des covariables ont également été obtenus (voir les tableaux S1 , S2 ; Figs. S1 , S2 ).
Les fréquences des patients dans chaque échantillon d'estimation et les taux d'infection au COVID-19 par les patients supplémentés par rapport aux patients témoins sont présentés dans le tableau 2 . Dans la cohorte vitamine D 3 , les taux de COVID-19 étaient de 2,66 % pour les traités et de 3,30 % pour les témoins, tandis que les taux d'infection au COVID-19 suivie d'un décès dans les 30 jours étaient de 0,23 % pour les traités et de 0,35 % pour les témoins. les contrôles. Dans la cohorte vitamine D 2 , les taux de COVID-19 étaient de 2,16 % pour les traités et de 2,97 % pour les témoins, tandis que les taux d'infection au COVID-19 suivie d'un décès dans les 30 jours étaient de 0,20 % pour les traités et de 0,26 % pour les témoins. les contrôles.
Tableau 2 Fréquences de COVID-19 par cohorte de patients après 1–1 appariement du score de propension.
Tableau pleine grandeur
Infections au COVID-19 dans l'échantillon total
Les patients supplémentés en vitamine D 3 et en vitamine D 2 pendant la période pandémique ont présenté une réduction associée de 20 % et 28 % du risque d'infection au COVID-19 par rapport aux témoins non traités (risque relatif D 3 (HR) = 0,80, [IC à 95 % 0,77, 0,83 ] ; D2HR = 0,72, [IC à 95 % 0,65, 0,79] ); voir Tableau 3 et Fig. 1 . Les associations de vitamine D résultantes étaient identiques à deux décimales après ajustement pour la saisonnalité.
Tableau 3 Estimations du rapport de risque.
Tableau pleine grandeur
Figure 1
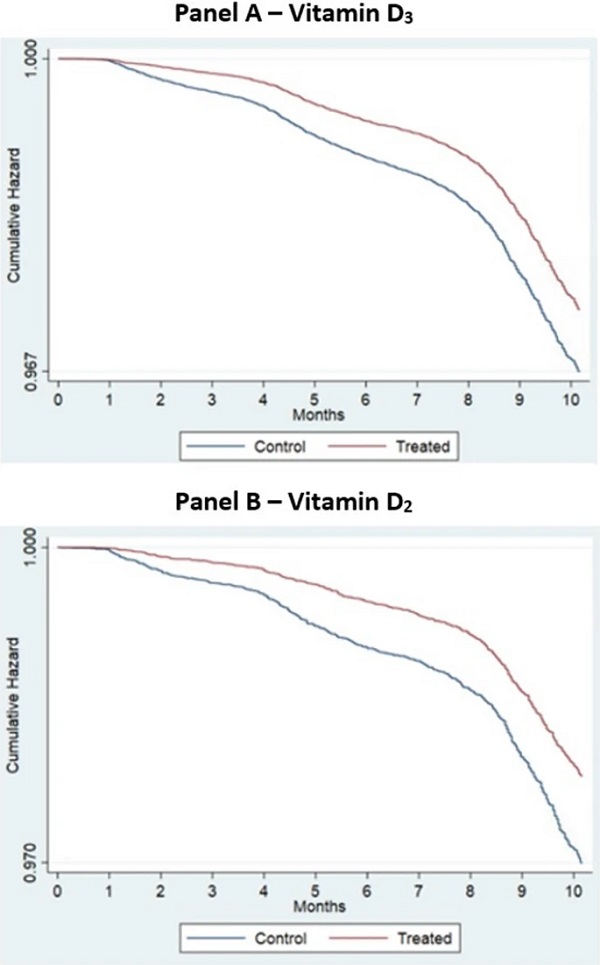
Courbes de Kaplan Meier pour les patients prenant des suppléments de vitamine D 3 et D 2 par rapport au groupe témoin - délai d'infection au COVID-19.
L'hypothèse nulle d'un modèle à risques proportionnels pour l'infection au COVID-19 sur la supplémentation en vitamine D a été rejetée (vitamine D 2 : Chi-Square = 13,98, df = 1, P < 0,001 ; vitamine D 3 : Chi-Square = 110,95, df = 1, P < 0,001).
Mortalité liée au COVID-19
La supplémentation en vitamine D 3 a été associée à un risque inférieur de 33 % d'infection au COVID-19 se terminant par une mortalité dans les 30 jours. (HR = 0,67, [IC à 95 % 0,59, 0,75]). Cependant, les résultats pour la vitamine D 2 étaient statistiquement non significatifs (HR = 0,75, [IC à 95 % 0,55, 1,04]) ; voir Tableau 3 et Fig. 2 . Les associations de vitamine D résultantes étaient identiques à deux décimales après ajustement pour la saisonnalité.
Figure 2
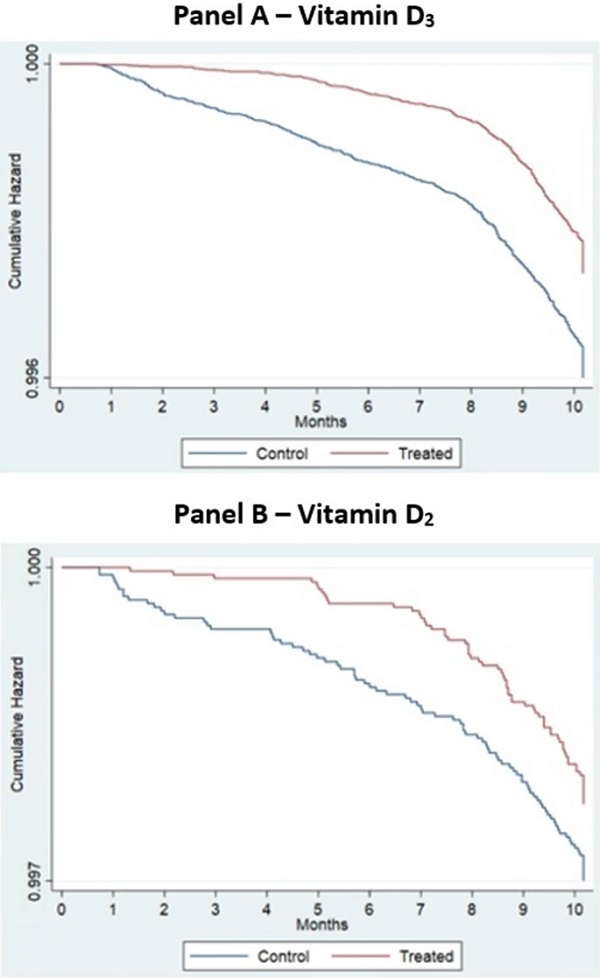
Courbes de Kaplan Meier pour les patients prenant des suppléments de vitamine D 3 et D 2 par rapport au groupe témoin - délai avant l'infection au COVID-19 se terminant par la mortalité dans les 30 jours.
L'hypothèse nulle d'un modèle à risques proportionnels pour l'infection au COVID-19 se terminant par le décès dans les 30 jours avec une supplémentation en vitamine D a été rejetée (vitamine D 2 : Chi-Square = 10,59, df = 1, P < 0,001 ; vitamine D 3 : Chi -Carré = 69,55, df = 1, P < 0,001).
Analyses de sous-groupes
Homme contre femme
Nous avons constaté une réduction associée similaire des taux d'infection au COVID-19 chez les patients masculins et féminins supplémentés en vitamine D 3 pendant la période pandémique (HR masculin = 0,80, [IC à 95 % 0,77, 0,83] ; HR féminin = 0,77, [IC à 95 % 0,68, 0,87]); voir Tableau 3 .
Noir contre blanc
Nous avons constaté une plus grande réduction associée des taux d'infection au COVID-19 chez les patients noirs que chez les patients supplémentés en blanc par rapport aux témoins (HR noir = 0,71, [IC à 95 % 0,65, 0,77] ; HR blanc = 0,82, [IC à 95 % 0,79, 0,86] ); voir Tableau 3 . L'interaction race par traitement était significative (HR = 0,86, [IC à 95 % 0,78, 0,94]). L'ajustement du taux sérique de vitamine D n'a pas modifié l'ampleur ou la signification de l'interaction course-traitement (HR = 0,85, [IC à 95 % 0,78, 0,94]).
0–19 ng/ml versus 20–39 ng/ml versus 40 + ng/ml taux sériques de vitamine D
Nous avons constaté que la réduction associée du risque d'infection au COVID-19 était inversement proportionnelle aux taux sériques de vitamine D (0–19 ng/ml : HR = 0,70, [IC à 95 % 0,64, 0,76] versus 20–39 ng/ml : HR = 0,81, [IC 95 % 0,77, 0,85] versus 40 + ng/ml : HR = 0,86, [IC 95 % 0,80, 0,92]) ; voir Tableau 3 . L'interaction globale entre le traitement et le niveau sérique de vitamine D était significative (HR = 1,12, [IC à 95 % 1,06, 1,18]), reflétant une augmentation de 12 % du rapport de risque (effet lié au traitement plus faible) avec chaque augmentation de la catégorie de niveau sérique.
Dose journalière cumulée et moyenne
Des relations dose-réponse significatives ont été trouvées pour la dose cumulée log e (HR = 0,981, [IC 95 % 0,978, 0,984]) et log edose quotidienne moyenne (HR = 0,969, [IC à 95 % 0,965, 0,974]). Ces rapports de risque sont pour un changement d'une unité logarithmique naturelle ; par conséquent, un triplement approximatif (augmentation de 2,718 fois) de la dose cumulée est associé à une réduction associée de 2 % du risque de COVD-19 et à une réduction associée de 3 % pour la dose quotidienne moyenne. Plus intuitivement, sur toute la gamme des doses cumulatives, cela représente une réduction associée de 25 % du risque de COVID-19 et une réduction associée de 27 % sur toute la gamme des doses quotidiennes moyennes. L'ampleur de la relation dose-réponse était inversement proportionnelle au taux sérique de vitamine D pour la dose cumulée (0–19 ng/ml : HR = 0,970, [IC à 95 % 0,963, 0,978] versus 20–39 ng/ml : HR = 0,982 , [IC 95 % 0,978, 0,986] versus 40 + ng/ml : HR = 0,987, [IC 95 % 0,981, 0,993]) et dose quotidienne moyenne (0–19 ng/ml : HR = 0,953, [IC 95 % 0,942 , 0. 965] versus 20–39 ng/ml : HR = 0,971, [IC 95% 0,965, 0,978] versus 40 + ng/ml : HR = 0,980, [IC 95% 0,970, 0,989]) ; Voir le tableau3 . Dans toute la gamme posologique, ces rapports de risque statistiquement significatifs représentent des réductions associées de 37 %, 24 % et 18 % pour la dose cumulative, et des réductions associées de 38 %, 25 % et 18 % pour la dose quotidienne moyenne. À une dose quotidienne moyenne de 50 000 UI, il y a eu une réduction associée de 49 % des infections au COVID-19 (HR = 0,51, [IC à 95 % 0,36, 0,70]) chez les patients présentant un faible taux sérique de vitamine D (0 à 19 ng/ml). niveaux.
Discussion
La supplémentation en vitamine D pendant la pandémie a été associée à une réduction significative de 20 % et 28 % des taux de COVID-19 confirmés en laboratoire pour la vitamine D 3 et la vitamine D 2, respectivement. La vitamine D 3 a été associée à une diminution significative de 33 % de la mortalité dans les 30 jours suivant l'infection au COVID-19. Cette diminution de la mortalité liée au COVID-19 est identique aux 33 % observés dans les données andalouses pour le calcifediol lorsqu'il est prescrit 15 jours avant l'hospitalisation et similaire à la réduction de la mortalité associée de 25 % pour le cholécalciférol (21). Pour la vitamine D2la réduction associée de la mortalité était de 25 % mais n'était pas statistiquement significative. Ces réductions de risque associées sont substantielles et justifient une exploration et une confirmation plus importantes à l'aide d'ECR. Ceci est particulièrement important compte tenu des taux élevés de carence en vitamine D dans la population américaine et du COVID-19.
Il y avait également des différences frappantes dans nos résultats entre nos sous-groupes de patients. Premièrement, par rapport aux patients blancs, les patients noirs supplémentés en vitamine D3 ont connu une réduction associée plus importante des taux d'infection au COVID- 19 par rapport aux témoins que les patients blancs (diminution de 29 % contre une diminution de 18 %). Des taux sériques inférieurs de vitamine D n'ont pas expliqué cette découverte. Pourtant, ces résultats suggèrent que l'expansion de la supplémentation en vitamine D pourrait potentiellement réduire les disparités raciales dans les résultats du COVID-19. Des recherches futures sont nécessaires pour déterminer le mécanisme par lequel la supplémentation en vitamine D est plus efficace chez les patients noirs.
Les taux sériques de base de vitamine D et la dose cumulée ont également modéré l'effet du traitement à la vitamine D 3 . Plus précisément, les patients ayant des taux sériques inférieurs recevant des doses plus élevées de vitamine D3 ont connu la plus grande réduction associée de l'infection. En réponse à ces résultats, les médecins pourraient envisager de prescrire régulièrement de la vitamine D 3 aux patients présentant des niveaux déficients pour les protéger contre l'infection au COVID-19 et la mortalité associée. La dose de 50 000 UI peut être particulièrement bénéfique.
Lorsque nous extrapolons nos résultats pour la supplémentation en vitamine D 3 à l'ensemble de la population américaine en 2020, il y aurait eu environ 4 millions de cas de COVID-19 en moins et 116 000 décès évités. Nous avons calculé ces valeurs en appliquant notre réduction moyenne estimée de 20 % de l'infection et de 33 % de la mortalité après infection pour la vitamine D 3 à un total de 19 860 000 cas et 351 999 décès jusqu'en 2020 (29). Dans la VA, il y a eu 343 094 cas et 14 981 décès connus jusqu'au 02/10/2021. En appliquant nos estimations à la VA, où il y aurait 69 000 cas de moins et 4 900 décès de moins entre mars 2020 et octobre 2021 (30). Ces calculs au dos de l'enveloppe peuvent être prudents étant donné les réductions possibles de la transmission du COVID-19 en raison de la réduction du risque pour la population générale due à une supplémentation plus large. À l'inverse, ces estimations peuvent également être gonflées si la population étudiée avait une prévalence plus élevée de faibles taux sériques de vitamine D que la population générale en raison de l'appariement des scores de propension à la supplémentation. Pourtant, compte tenu de nos découvertes, de l'absence d'effets secondaires graves et de la disponibilité généralisée de la vitamine D 3 à faible coût, la vitamine D 3 présente une opportunité unique de réduire la propagation et la gravité de la pandémie de COVID-19.
Limites
Malgré un appariement réussi des patients témoins, il peut encore y avoir une confusion résiduelle. Patients ayant fait le plein de vitamine D 3 ou D 2les prescriptions peuvent avoir de meilleurs résultats que d'autres si la supplémentation est associée à un meilleur accès aux soins ou à la recherche proactive de soins, aux soins personnels et à des comportements spécifiques à la prévention de la COVID-19 (c.-à-d. distanciation sociale et port de masque) que les contrôles. Alternativement, les patients supplémentés peuvent être plus susceptibles de vivre dans des climats plus froids où la carence en vitamine D et les taux de COVID-19 étaient élevés en 2020. Il existe également de nombreux facteurs importants que nous n'avons pas pu contrôler dans notre analyse statistique qui sont associés à COVID-19 l'infection et la mortalité, y compris le statut socio-économique et le poids/l'obésité. Pourtant, ces préoccupations sont atténuées par les associations significatives entre de faibles taux sériques de vitamine D et des doses moyennes et cumulatives plus élevées avec de meilleurs résultats.
En plus de la confusion résiduelle, nos résultats peuvent souffrir d'un biais de mesure. De nombreux cas de COVID-19, en particulier au début de la période pandémique, n'ont pas été diagnostiqués en raison d'un manque de tests disponibles. Par conséquent, certains anciens combattants infectés qui ont reçu des soins pour leurs symptômes dans le VA ou Medicare n'ont peut-être pas été diagnostiqués. De même, les cas positifs identifiés par des prestataires non VA et non Medicare peuvent ne pas être observés. Notre association serait surestimée si les patients supplémentés en vitamine D étaient sous-diagnostiqués de manière disproportionnée par rapport aux patients témoins. En effet, les patients présentant des infections non détectées seraient peu susceptibles d'être réinfectés lorsque la disponibilité des tests augmenterait plus tard au cours de notre période d'étude. Deuxième, notre mesure du COVID-19 se terminant par un décès dans les 30 jours pourrait également être inexacte car nous n'avions pas accès aux données du certificat de décès pour confirmer la cause réelle du décès. Cependant, de nombreux décès immédiatement après l'infection au COVID-19 sont susceptibles d'être au moins partiellement liés.
La disponibilité de la vitamine D 3 sans ordonnance limite également notre capacité à nous assurer que nous avons entièrement catégorisé le dosage et l'intensité de la supplémentation. Nous avons peut-être mal classé les patients qui recevaient de la vitamine D 3 en vente libre comme témoins. Au contraire, les prescriptions de suppléments peuvent être remplies par des anciens combattants qui ne finissent pas par les prendre, ce qui rend certains patients traités plus similaires aux témoins. À ces égards, nos estimations représenteraient des limites inférieures sur l'impact réel de la vitamine D 3 .
Nous notons que les tests de risques proportionnels pour le modèle de risque d'infection COVID-19 et le risque d'infection se terminant par la mort dans les 30 jours étaient significatifs, indiquant un manque de proportionnalité de l'association de supplémentation en vitamine D. Cependant, une inspection des courbes de Kaplan-Meier dans les Figs. 1 et 2 révèlent peu ou pas de différence entre les anciens combattants supplémentés et témoins au cours du premier mois de traitement (c'est-à-dire en mars 2020, lorsque la pandémie a commencé), qui augmente régulièrement dans les trois mois suivant le suivi et est relativement constante par la suite. Ces différences expliquent la non-proportionnalité de l'association supplémentation en Vitamine D.
Nos découvertes peuvent également ne pas se généraliser à de nouvelles variantes, telles que la variante delta COVID-19 qui est devenue dominante à la mi-2021. La variante delta se propage plus rapidement et est plus mortelle que les variantes qui existaient pendant notre période d'étude, ce qui peut affaiblir les associations que nous avons observées. Des recherches supplémentaires avec des données mises à jour seront nécessaires pour établir la pertinence continue de nos découvertes pour les nouvelles variantes, y compris l'omnicron. Cependant, étant donné la capacité des vaccins à prévenir l'infection par la variante delta et les similitudes biologiques entre la variante delta et les souches précédentes, nous espérons que nos résultats s'étendront au moins en partie aux nouvelles variantes. Néanmoins, la période utilisée dans notre étude a l'avantage de précéder la disponibilité générale des vaccins et donc de
Enfin, nos résultats sont des associations. Des ECR sont finalement nécessaires pour établir un lien de causalité entre la supplémentation en vitamine D 3 et D 2 et l'infection au COVID-19 et la mort. Suite aux résultats des ECR, nos découvertes aideront à conférer la généralisabilité des résultats des ECR à de larges populations de patients du monde réel.
Conclusion
Chez les patients AV, la vitamine D 3 et la vitamine D 2la supplémentation a réduit le risque associé d'infection au COVID-19 de 20 % et 28 %, et l'infection au COVID-19 se terminant par un décès dans les 30 jours de 33 % et 25 %. Les anciens combattants noirs recevant une supplémentation présentaient une réduction associée plus importante que les blancs, bien que les deux soient statistiquement significatifs et que la différence ne soit pas expliquée par les différences de taux sériques de vitamine D. Les patients avec de faibles taux de vitamine D au départ ont davantage bénéficié de la supplémentation que les patients avec des taux sériques plus élevés. Enfin, les patients recevant des doses cumulatives plus élevées et des doses quotidiennes moyennes plus élevées présentaient une réduction associée plus importante des taux d'infection au COVID-19 que les patients recevant des doses plus faibles sous réserve de taux sériques similaires de vitamine D. La relation dose-réponse la plus importante a été observée chez les patients ayant les taux sériques de vitamine D les plus bas. En tant que largement disponible,3 pourrait être un outil utile pour réduire la propagation de l'infection au COVID-19 et la mortalité associée et réduire les disparités raciales dans les résultats du COVID-19. Nos résultats sont particulièrement pertinents pour la population américaine, étant donné qu'environ la moitié des Américains auraient des taux sériques de vitamine D sous-optimaux.
Disponibilité des données
Les données qui étayent les conclusions de cette étude sont disponibles auprès du Département des anciens combattants des États-Unis, mais des restrictions s'appliquent à la disponibilité de ces données, qui ont été utilisées pour l'étude actuelle, et ne sont donc pas accessibles au public. Les données sont cependant disponibles auprès des auteurs sur demande raisonnable et avec l'autorisation du Département américain des anciens combattants.
Références:
-
Forrest, KY & Stuhldreher, WL Prévalence et corrélats de la carence en vitamine D chez les adultes américains. Nutr. Rés. 31 (1), 48–54. https://doi.org/10.1016/j.nutres.2010.12.001 (2011).
-
Meltzer, DO et al. Association du statut en vitamine D et d'autres caractéristiques cliniques avec les résultats des tests COVID-19. Réseau JAMA. Ouvert. 3 (9), e2019722. https://doi.org/10.1001/jamanetworkopen.2020.19722 (2020).
-
Maghbooli, Z. et al. Une suffisance en vitamine D, un taux sérique de 25-hydroxyvitamine D d'au moins 30 ng/mL réduit le risque de résultats cliniques indésirables chez les patients infectés par le COVID-19. PLoS ONE 15 (9), e0239799. https://doi.org/10.1371/journal.pone.0239799 (2020).
-
Kaufman, HW, Niles, JK, Kroll, MH, Bi, C. & Holick, MF Taux de positivité du SRAS-CoV-2 associés aux taux de 25-hydroxyvitamine D en circulation. PLoS ONE 15 (9), e0239252. https://doi.org/10.1371/journal.pone.0239252 (2020).
- Source : Nature